Teknisk studentereksamen

Dette prøvesæt er omfattet af ophavsretten, jf. ophavsretslovens § 1.
Prøvesættet må alene anvendes til den på prøvesættet anførte prøve.
Al anden anvendelse af prøvesættet, herunder visning eller deling f.eks. via internettet, sociale medier, portaler og bøger, udgør en krænkelse af Børne- og Undervisningsministeriets og evt. tredjemands ophavsret og er ikke tilladt.
Overtrædelse af ophavsretten kan være erstatningspådragende og/eller strafbart.
Prøvesættet kan dog, efter at prøven er afsluttet, anvendes til undervisningsbrug på uddannelser m.v. omfattet af den lovgivning, som Styrelsen for Undervisning og Kvalitet administrerer.
Opgave 4 - Fluorethansyre
Fluorethansyre anvendes til fremstilling af en række forskellige fluorholdige pesticider. Det forekommer blandt andet i den giftige sydafrikanske plante Dichapetalum cymosum, hvor stoffet er ansvarlig for plantens giftighed. Strukturformler for ethansyre, fluorethansyre, difluorethansyre og trifluorethansyre ses på figur 4.1.
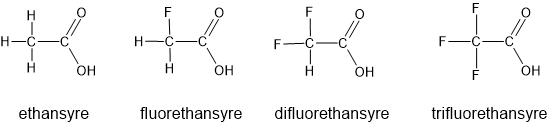
Figur 4.1. Strukturformler for ethansyre, fluorethansyre, difluorethansyre og trifluorethansyre
Fluorethansyre ekstraheres fra planten med 1,00 L demineraliseret vand. Indholdet af fluorethansyre i ekstraktet blev bestemt til 0,00164 mol/L.
| a) | Beregn massen af fluorethansyre i ekstraktet. |
Syrestyrken for syrerne vist i figur 4.1 afhænger af antallet af fluoratomer. Tabel 4.1 viser pKs-værdierne for disse fire syrer ved 25 °C.
| ethansyre | fluorethansyre | difluorethansyre | trifluorethansyre | |
| pKs | 4,76 | 2,59 | 1,33 | 0,23 |
Tabel 4.1 pKs-værdierne for ethansyre, fluorethansyre, difluorethansyre og trifluorethansyre ved 25 °C.
| b) | Beregn pH i ekstraktet ved 25 °C. |
| c) | Forklar, hvorfor pKs-værdierne vist i tabel 4.1 falder med stigende antal fluoratomer. |
Opgave 3 - Gingerol
| Gingeroler findes blandt andet i ingefær, og den stærke smag af ingefær skyldes stoffets binding til smertereceptorer på tungen. Når man tørrer ingefær omdannes 6-gingerol til 6-shogaol. Figur 3.3 viser omdannelse af 6-gingerol til 6-shogaol. 6-shogaol er cirka dobbelt så stærk som 6-gingerol, hvilket er årsagen til at ingefærpulver er stærkere end frisk ingefær. Strukturformler for tre forskellige gingeroler og 6-shogaol ses på figur 3.2 og kan ses her som henholdsvis Marvinsketch- og ChemSketch-fil. |
 Figur 3.1 Ingefær Figur 3.1 Ingefær |
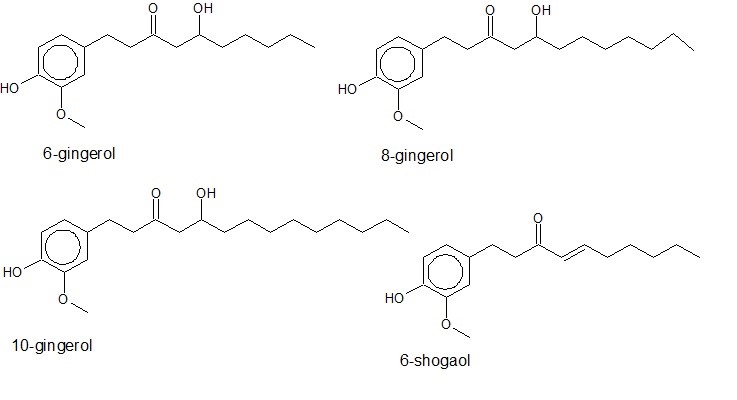
|
| Figur 3.2 Strukturformler for tre gingeroler og en shogaol |
| a) | Argumenter for at 6-shogaol findes på to stereoisomere former. |
Ved tørring af ingefær, hvor 6-gingerol omdannes til 6-shogaol sker der en omdannelse i hybridisering af flere carbonatomer. Et af disse carbonatomer er markeret med rød cirkel i figur 3.3.
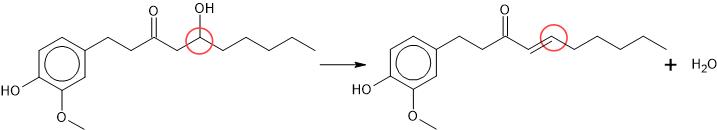
|
| Figur 3.3 Reaktionsskema for omdannelse af 6-gingerol til 6-shogaol |
| b) | Angiv reaktionstype for omdannelsen af 6-gingerol til 6-shogaol. Begrund dit svar med udgangspunkt i figur 3.3. |
| c) | Redegør for ændringen i hybridisering af det markerede carbonatom under omdannelsen af 6-gingerol til 6-shogaol. |
Indholdet af gingeroler i ingefær bestemmes ved HPLC. Den mobile fase er polær og kolonnen er upolær. Animationen viser analysen af ingefærekstrakt.
| d) | Opskriv en tabel med resultaterne fra HPLC-analysen af ingefærekstrakt. Analysér retentionstiderne fra HPLC-analysen. Inddrag strukturformlerne vist på figur 3.2. |
En gruppe forskere vil undersøge indholdet af 6-gingerol i frisk ingefær ved hjælp af HPLC-analysen vist i animationen. Som forberedelse til undersøgelsen fremstilles en standardkurve. Data til standardkurven ses her som Excel-fil.
1,003 g frisk ingefær afvejes og ekstraheres med 100,0 mL methanol. Denne prøve behandles på samme måde som opløsninger til standardkurven. Arealet af ingefæropløsningen bestemmes til 507,95.
| e) | Afbild standardkurven. Beregn indholdet af 6-gingerol i frisk ingefær. Resultatet skal angives i µg/g ingefær. |
Opgave 2 - Mangan(2+)hydroxid
Mangan(2+)hydroxid, Mn(OH)2, er en tungtopløselig ionforbindelse. Opløselighedsligevægten for mangan(2+)hydroxid ses af figur 2.1.
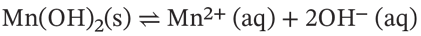
Figur 2.1 Opløselighedsligevægten for mangan(2+)hydroxid
| a) | Opskriv ligevægtsloven, Ko, for reaktionen vist i figur 2.1. |
Ligevægtskonstanten for reaktionen vist i figur 2.1 er bestemt ved forskellige temperaturer og ses i tabel 2.1.
| t (°C) | 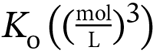 |
| 25 | 0,696 |
| 35 | 0,883 |
| 45 | 1,01 |
| 55 | 1,19 |
Tabel 2.1 Sammenhørende værdier mellem ligevægtskonstanten og temperaturen for reaktionen vist i figur 2.1
| b) | Vurder, om reaktionen mod højre er endoterm eller exoterm. Benyt tabel 2.1. |
Der fremstilles en mættet vandig opløsning af mangan(2+)hydroxid ved 25 °C.
| c) | Beregn den aktuelle stofmængdekoncentration af henholdsvis Mn2+ og OH- i den mættede opløsning. |
| d) | Redegør for, om opløseligheden af mangan(2+)hydroxid er størst i en sur opløsning eller i vand. |
Spørgsmålene i opgave 1 tager udgangspunkt i bilagsmaterialet.
Opgave 1 - Polyester
| a) | Beregn omdannelsesprocenten i forsøg 1A med hjortetakssalt. |
| b) | Angiv det systematiske navn for hjortetakssalt. |
| c) | Markér to forskellige funktionelle grupper i BHET. Angiv stofklasser for de markerede funktionelle grupper. |
| d) | Argumentér for reaktionsordnen for reaktionen vist i figur 1.2 ved 200 °C. Inddrag figur 1.3. Bestem hastighedskonstanten, k, for reaktionen. |
| e) | Vis, at aktiveringsenergien for reaktionen vist i figur 1.2 med hjortetakssalt som katalysator er 146 kJ/mol. |
| f) | Argumentér for, hvilken af de to katalysatorer der giver den højeste reaktionshastighed for reaktionen vist i figur 1.2. |
Bilagsmateriale - Polyester
Polyester, der er en fællesbetegnelse for forskellige typer af plast som for eksempel PET (polyethylenterephtalat), er et af de mest benyttede materialer til forskellige former for tekstiler. En af de største udfordringer med polyester er bortskaffelsen af materialet, når tekstilprodukterne er slidt ned. Af forskellige årsager er polyester svært at genanvende, og derfor var det opsigtsvækkende, da kemikere fra blandt andet Københavns Universitet i 2023 offentliggjorde et forskningsprojekt, hvor de beskriver, hvordan PET kan nedbrydes og dermed lettere kan genanvendes.

Figur 1.1 PET anvendes blandt andet til forskellige tekstilprodukter.
Plast består af polymerer, og metoden går blandt andet ud på at nedbryde polymeren til monomerer. PET kan nedbrydes til monomeren BHET (bis(2-hydroxyethyl)terephtalat). Reaktionsskemaet for nedbrydningen ses af reaktionen i figur 1.2:
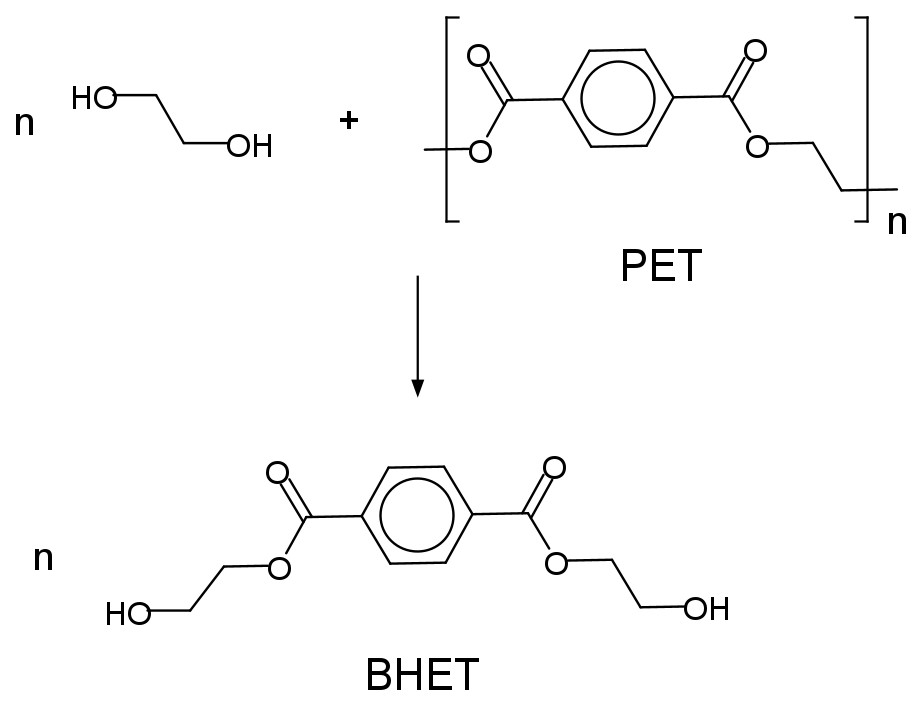
Figur 1.2 Reaktionen hvor PET nedbrydes til BHET. Symbolet n i reaktionen angiver antallet af monomer i PET og antallet af de øvrige molekyler i reaktionsskemaet og har typisk en størrelse mellem 100-200.
For at optimere processen har forskerholdet gennemført en række forsøg med forskellige katalysatorer. Forsøgene har blandt andet undersøgt omdannelsesprocenter og reaktionshastigheder ved brugen af forskellige katalysatorer. De to bedste katalysatorer har vist sig at være zinkchlorid, ZnCl2, og hjortetakssalt, NH4HCO3. Hjortetakssalt er en almindelig køkkeningrediens.
I tabel 1.1 ses data med omdannelsesprocenter fra to forsøg med omdannelsen af PET til BHET. Omdannelsesprocent er beregnet ved anvendelse af formel 1.1.
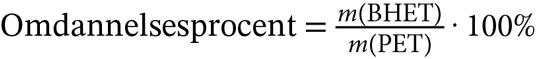 |
Formel (1.1) |
Forsøg |
Katalysator | Masse af PET (g) |
Masse af BHET (g) |
Omdannelsesprocent (%) |
| 1A | Hjortetakssalt | 2.00 | 1,68 | |
| 1B | Zinkchlorid | 2,00 | 0,66 | 33 |
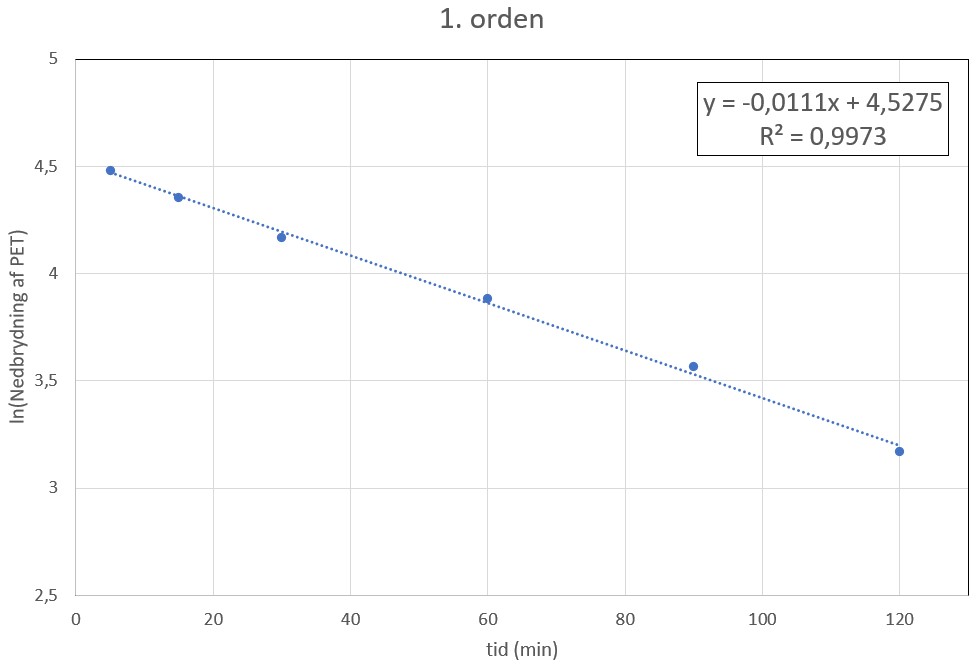
I et andet forsøg undersøges reaktionen vist i figur 1.2 ved 200 oC for at bestemme reaktionens orden. Resultaterne fra forsøget med hjortetakssalt som katalysator kan ses på figur 1.3.
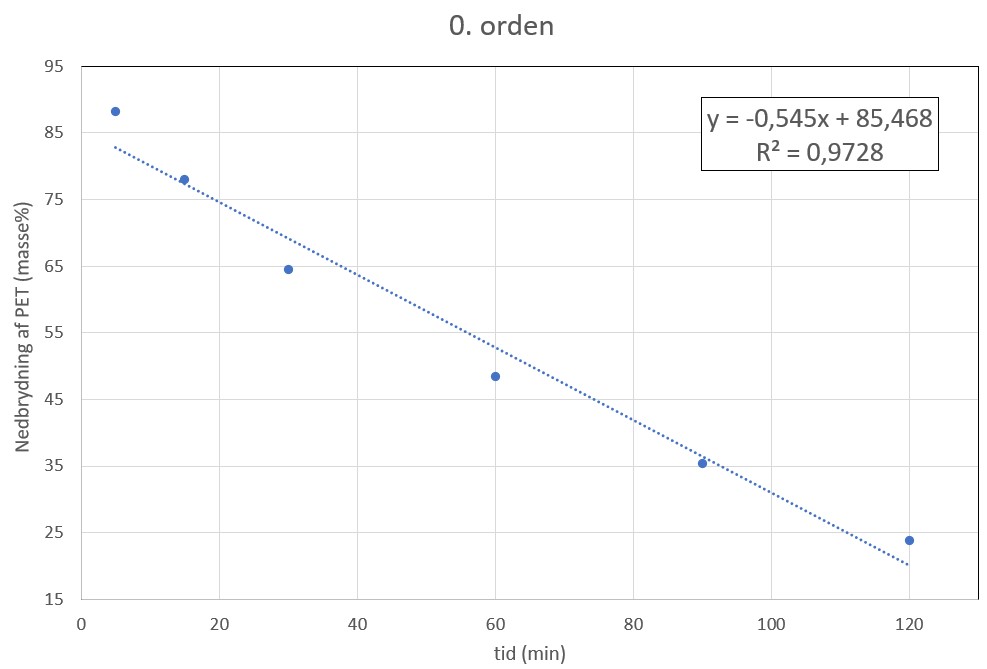 |
 |
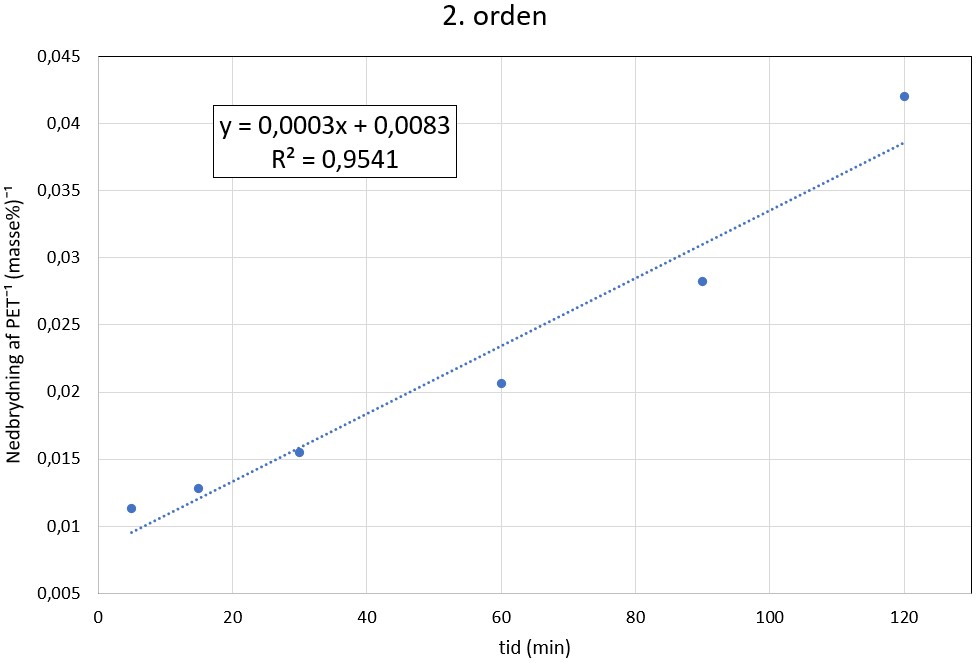 |
| Figur 1.3 Tre grafer som undersøger reaktionsordenen af nedbrydning af PET til BHET med hjortetakssalt som katalysator. |
I et tredje forsøg undersøges reaktionens aktiveringsenergi nærmere. Dette gøres ved at bestemme hastighedskonstanten ved tre andre temperaturer. Ved brug af zinkclorid som katalysator er aktiveringsenergien blevet bestemt til 84 kJ/mol. Data fra eksperimentet med hjortetakssalt som katalysator ses i Excel-fil.
Vejledning
Følgende hjælpemidler forudsættes:
DATABOG fysik kemi (F&K Forlaget), 11. udgave (2007) eller senere udgave.
Opgavebesvarelsen
Din opgavebesvarelse skal afleveres i et samlet dokument gemt i pdf-format.
Bedømmelse
Ved den skriftlige prøve lægges der vægt på din evne til at:
| - | anvende fagets viden og metoder til behandling af kemiske problemstillinger | |
| - | inddrage det udleverede bilagsmateriale i besvarelsen | |
| - | gøre iagttagelser og analysere eksperimentelt arbejde, samt efterbehandle og vurdere resultater herfra | |
| - | gennemføre og præsentere relevante beregninger med korrekt brug af fagsprog | |
| - | benytte relevante matematiske modeller, metoder og repræsentationsformer | |
| - | benytte fagspecifikke digitale værktøjer hensigtsmæssigt | |
| - | dokumentere anvendte informationer fra forskellige kilder | |
| - | udtrykke sig skriftligt, således at tankegangen fremstår struktureret og tydelig. |
Der gives en karakter på baggrund af en helhedsvurdering.
Kemi A
Mandag den 2. juni 2025
2. del
Kl. 9.30-14.30